Dalam bidang ilmu kimia, reaksi esterifikasi merupakan salah satu fenomena yang menarik dan penting untuk kita pelajari. Reaksi ini melibatkan penggabungan antara asam karboksilat dan alkohol untuk membentuk senyawa kimia bernama ester.
Namun, apakah Anda tahu bahwa reaksi ini sangat berguna untuk berbagai macam bidang? Jika belum, simak artikel ini yang akan menjelaskan tentang konsep, cara reaksi, dan contoh nyata esterifikasi dalam kehidupan.
Apa Itu Reaksi Esterifikasi?
Singkatnya, reaksi esterifikasi adalah reaksi kimia yang terjadi antara senyawa alkohol (ROH) dan jenis senyawa asam tertentu, terutama asam karboksilat (RCOOH), untuk menghasilkan ester (RCOOR) dan air.
Bagi yang belum familiar, produk ester adalah senyawa kimia dengan dua gugus karbon yang terikat pada atom oksigen. Produksi ester juga dapat berasal dari reaksi antara asil klorida (asam klorida) dan alkohol serta dari anhidrida asam dan alkohol.
Jenis-jenis Metode Reaksi Esterifikasi
Esterifikasi dapat terjadi dalam tiga cara, yaitu:
1. Reaksi Esterifikasi antara Asam Klorida dan Alkohol
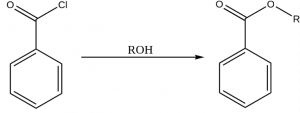
Reaksi esterifikasi dapat dilakukan dengan mereaksikan alkohol dan asam klorida pada suhu kamar. Ester dapat Anda peroleh dengan asap asam hidrogen klorida yang beruap. Misalnya, benzoil klorida dan alkohol bereaksi membentuk ester.
2. Reaksi Esterifikasi antara Asam Anhidrida dan Alkohol
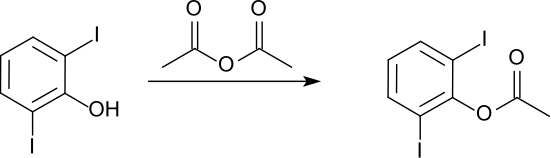
Reaksi antara alkohol dan asam anhidrida relatif lebih lambat bila Anda bandingkan dengan asam klorida. Sehingga, untuk mendapatkan sejumlah ester, Anda perlu menghangatkan campuran untuk mendapatkan lebih banyak ester. Senyawa 2,6 – diiodophenol dengan asam anhidrida adalah salah satu contoh pembentukan ester.
3. Reaksi Esterifikasi antara Asam Karboksilat dan Alkohol
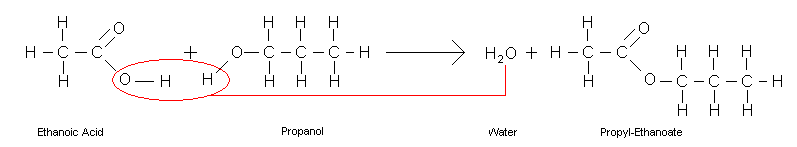
Reaksi antara asam karboksilat dan alkohol untuk produksi ester melibatkan proses pemanasan dengan adanya katalis asam seperti asam sulfat (H2SO4). Misalnya, reaksi asam etanotat dan propanol untuk membentuk propil etanoat dan air.
Reaksi Esterifikasi Menghasilkan Produk Ester
Berdasarkan ketiga metode produksi ester yang telah kita bahas di atas, berikut adalah sejumlah contoh produksi ester dari reaksi antara asam karboksilat dan alkohol dalam dua skala:
1. Dalam Skala Tabung Reaksi
Proses terbentuknya ester dapat Anda amati saat asam karboksilat dan alkohol dipanaskan bersama setelah ditambahkan beberapa tetes asam sulfat pekat sebagai katalis. Hasil dari reaksi ini akan terlihat dengan munculnya aroma buah, yang mengindikasikan terjadinya pembentukan ester.
Untuk pengamatan yang lebih cepat, Anda dapat menggunakan sejumlah kecil dari keseluruhan campuran dalam tabung reaksi. Lalu, panaskan dalam bak air panas selama beberapa menit.
Indikasi aroma sering terdistorsi oleh bau asam karboksilat karena reaksi sebaliknya untuk membentuk asam karboksilat. Dengan menuangkan seluruh campuran reaksi ke dalam gelas kimia kecil, baunya dapat terdeteksi.
Ester cukup mudah larut dalam air tetapi kelarutannya akan berkurang seiring dengan bertambahnya panjang rantai. Ester rantai panjang membentuk lapisan tipis di permukaan.
Asam dan alkohol masing-masing larut dalam air dan tersimpan dengan aman di bawah lapisan ester. Ester rantai panjang akan berbau, cenderung ke arah penyedap buah buatan.
2. Dalam Skala yang Lebih Besar
Produksi ester dalam reaksi esterifikasi dengan skala besar terbagi menjadi dua metode berbeda, yaitu ester rantai pendek dan panjang. Ester dengan rantai pendek biasanya akan terbentuk lebih cepat daripada rantai panjang.
Salah satu contohnya adalah dengan memanaskan campuran asam etanoat dan etanol dengan adanya asam sulfat pekat sebagai katalis, maka asam etanoat ester rantai pendek dapat dibuat. Kemudian, campuran mentah melalui proses penyulingan untuk mendapatkan ester dalam bentuk murni.
Penyulingan campuran reaksi untuk menghasilkan ester bertujuan mencegah reaksi balik terjadi. Ester rantai pendek tidak memiliki ikatan hidrogen, gaya antar molekul terlemah dan dengan demikian titik didih terendah apabila Anda bandingkan dengan unsur-unsur lain dalam campuran reaksi.
Jadi, dengan adanya proses distilasi, Anda dapat dengan mudah memisahkan ester dari campuran reaksi. Oleh karena itu, reaksi kesetimbangan dengan mengeluarkan produk dari campuran reaksi dengan cara penyulingan dapat meningkatkan produksi ester.
Ester dengan rantai yang panjang akan lebih lambat daripada ester rantai pendek. Reaksi perlu pemanasan di bawah refluks selama beberapa waktu untuk menghasilkan campuran kesetimbangan. Produk ester dapat terpisahkan dari campuran reaksi kesetimbangan dengan distilasi fraksional.
Mekanisme Reaksi Esterifikasi
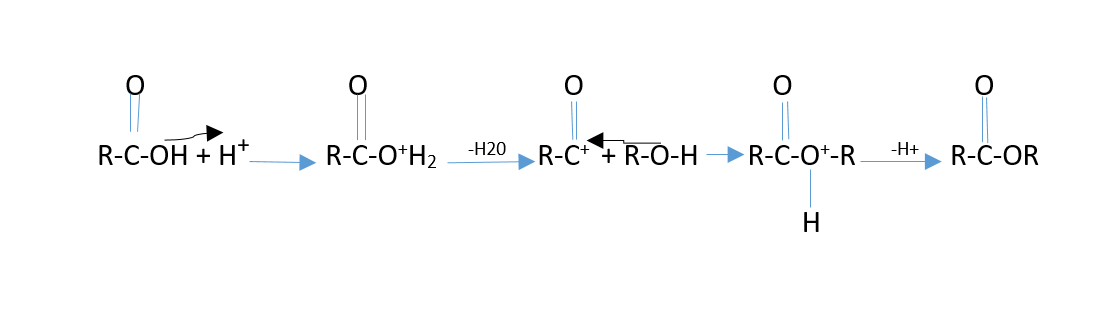
Mekanisme esterifikasi terdiri dari lima tahap yang memiliki prosedurnya masing-masing. Berikut ini penjelasannya:
1. Pembentukan Kation
Langkah pertama melibatkan asam etanoat yang menyerap proton (ion hidrogen) dari asam sulfat pekat. Proton ini berikatan dengan salah satu pasangan oksigen soliter yang terikat ganda pada karbon.
2. Karbonasi Terdelokalisasi
Karbonasi dapat menggunakan metanol yang berfungsi sebagai nukleofil. Metanol biasanya hadir secara berlebihan dalam reaksi ini, sehingga perlu Anda ingat bahwa ada banyak molekul dalam larutan.
Pada tahap reaksi esterifikasi ini, oksigen karboksil terprotonasi, sehingga menghasilkan karbokation terdelokalisasi yang membuat karbokation menjadi elektrofil yang lebih besar.
3. Transfer Proton
Ester yang terprotonasi akan menguap sebagai metanol, tetapi tidak menghasilkan senyawa apa pun. Sebuah proton akan bertransfer ke salah satu gugus hidroksil, yang membuatnya menjadi gugus yang sangat baik.
4. Membentuk Ikatan Pi
Atom oksigen alkohol dari gugus hidroksil memberikan sepasang elektron ke atom karbon dan membentuk ikatan dengan memindahkan molekul air. Air tidak dapat membalikkan proses secara efektif karena konsentrasinya rendah apabila Anda bandingkan dengan konsentrasi metanol.
Sehingga, air yang hilang bukanlah nukleofil yang cocok untuk membalikkan reaksi. Konsentrasi air yang Anda butuhkan untuk membalikkan seluruh proses sangat rendah.
5. Pembentukan Ester
Dari beberapa tahap sebelumnya, tahap akhir dari mekanisme reaksi esterifikasi akan terbentuk ester sebagai hasil produksinya. Tahap ini menandai keberhasilan transformasi bahan kimia dasar menjadi senyawa yang lebih kompleks dan beragam.
Sifat-sifat Ester
Beberapa sifat ester dari reaksi esterifikasi adalah sebagai berikut:
1. Titik Didih
Titik didih ester mirip dengan aldehida dan keton dengan jumlah atom karbon yang sama. Senyawa ester, seperti aldehida dan keton, adalah senyawa polar dengan interaksi dipol-dipol dan gaya dispersi van der Waals.
Mereka tidak membentuk ikatan hidrogen ester-ester. Sehingga, titik didihnya akan jauh lebih rendah daripada asam dengan jumlah atom karbon yang sama.
2. Kelarutan Air
Banyak kelarutan ester dalam lipid dan air merupakan karakteristik fisik yang penting. Senyawa ester yang merupakan hasil produksi reaksi esterifikasi akan larut dalam air karena hubungan oksigen-karbon polar, sehingga dapat berpartisipasi dalam ikatan hidrogen.
Hidrogen bermuatan positif dalam molekul air akan tertarik ke oksigen bermuatan negatif dalam molekul ester. Ester rantai pendek sangat larut dalam air, tetapi ketika molekul ester menjadi rantai yang lebih panjang, ia menjadi kurang larut dalam air.
Ketika rantai ester menjadi terlalu panjang, maka komponen hidrokarbon mulai memutus ikatan hidrogen antara molekul air.
3. Titik Lebur
Titik lebur suatu bahan menentukan apakah senyawa itu lemak atau minyak. Rantai jenuh adalah umum dalam lemak. Kondisi ini memungkinkan gaya dispersi van der Waals yang lebih efektif antara molekul yang membutuhkan lebih banyak energi untuk memutus rantai dan meningkatkan titik leleh.
Kegunaan Ester Hasil Produksi Reaksi Esterifikasi

Berikut ini adalah beberapa kegunaan ester:
1. Parfum
Berhubung aroma inheren ester bersifat harus, ester populer di kalangan pembuat parfum dan pembuat produk perawatan pribadi. Misalnya, Propyl Ethonoate berbau seperti sepasang sepatu segar, Pentyl Nonoate berbau seperti bunga, dan Propyl Octanoate berbau seperti kelapa.
2. Pelarut
Kebermanfaatan ester juga dapat berguna sebagai pelarut. Pelarut yang berfungsi untuk melarutkan zat memungkinkan molekul larutan untuk bercampur dan berfungsi secara efektif. Untuk mencapai konsistensi yang benar, banyak produk perawatan pribadi, seperti bubuk, lotion, dan krim cukur termasuk dalam pelarut.
3. Lotion
Memberi manfaat bagi kulit, produk ester memiliki sifat sebagai emolien yang mampu menjaga kelembapan dan kelembutan kulit. Emolien adalah senyawa aktif dalam krim dan lotion yang berfungsi untuk menghaluskan tekstur kulit.
Kelebihan dari ester daripada jenis emolien lainnya adalah ester tidak meninggalkan residu berminyak pada kulit. Sehingga, produk dari reaksi esterifikasi ini dapat memberikan manfaat.
Sudahkah Anda Paham dengan Reaksi Esterifikasi?
Dalam kesimpulannya, reaksi esterifikasi adalah proses penting dalam kimia organik dengan berbagai aplikasi di berbagai industri. Dengan menggabungkan asam karboksilat dan alkohol, maka ester terbentuk.
Hasil produksi ester memberikan aroma, rasa, dan karakteristik unik pada banyak produk yang kita gunakan sehari-hari. Mulai dari makanan hingga parfum, reaksi esterifikasi memainkan peran penting dalam menciptakan pengalaman sensorik yang beragam.
Dengan pemahaman lebih mendalam tentang mekanisme reaksi dan contoh-contoh penerapannya, maka Anda dapat lebih menghargai kompleksitas kimia di balik senyawa ester yang sering Anda temui.

