Dalam ilmu kimia, Anda akan menemukan berbagai istilah dan konsep penting untuk memahami sifat dan perilaku materi. Salah satunya adalah konsep molekul senyawa yang mana merujuk pada salah satu komponen dasar dalam kimia yang membentuk materi di sekitar kita.
Jika Anda sedang mempelajari molekul dan zat-zat kimia dalam kehidupan sehari-hari, maka simak artikel ini. Sebab, di sini, kita akan membahas pengertian, sifat, ciri, manfaat, serta memberikan contoh-contoh molekul senyawa yang berbeda dengan molekul unsur.
Pengertian dan Konsep Molekul Senyawa
Molekul senyawa atau senyawa kimia terbentuk ketika dua atau lebih atom dari unsur yang berbeda terikat bersama melalui ikatan kimia. Jadi, senyawa kimia adalah materi dari gabungan berbagai unsur kimia dalam komposisi tertentu.
Dalam setiap senyawa, atom-atom unsur tersebut bergabung dan membentuk susunan yang unik, yang pada gilirannya menentukan sifat dan karakteristik senyawa tersebut.
Anggaplah atom sebagai “bata bangunan” dasar yang membentuk materi. Namun, atom tidak selalu berdiri sendiri; mereka dapat berikatan dengan atom lain untuk membentuk molekul. Sementara molekul senyawa adalah hasil dari interaksi tersebut.
Terutama ketika atom-atom bergabung untuk membentuk struktur yang lebih besar dengan sifat-sifat yang berbeda dari unsur yang membentuknya. Misalnya, molekul air (H2O) terdiri dari dua atom hidrogen (H) dan satu atom oksigen (O) yang terikat bersama melalui ikatan kovalen.
Pada anggapan di atas, atom hidrogen dan oksigen berkontribusi pada pembentukan molekul air. Selain itu, ikatan atom-atom tersebut membuat air memiliki sifat-sifat unik, seperti titik didih dan titik leleh tertentu, serta kemampuan untuk membentuk ikatan hidrogen dengan molekul-molekul lain.
Senyawa adalah dasar dari materi yang Anda temui sehari-hari. Semua benda padat, cair, atau gas terdiri dari berbagai molekul senyawa. Bahkan, beberapa senyawa kimia dapat terdiri dari beberapa puluh hingga jutaan atom yang terikat bersama dalam pola yang kompleks.
Perbedaan Molekul Senyawa dan Molekul Unsur
Senyawa dan unsur kimia memiliki perbedaan yang mencolok dalam hal struktur, komposisi, dan sifat. Berikut adalah perbandingan antara keduanya:
1. Komposisi Atom
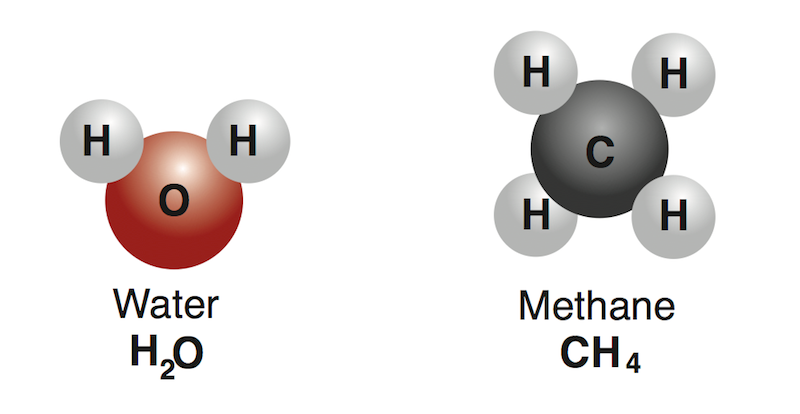
Senyawa kimia terbentuk oleh dua atau lebih atom dari unsur yang berbeda yang terikat bersama melalui ikatan kimia. Proses pembentukan senyawa ini melibatkan pertukaran, berbagi, atau transfer elektron antara atom-atom tersebut.
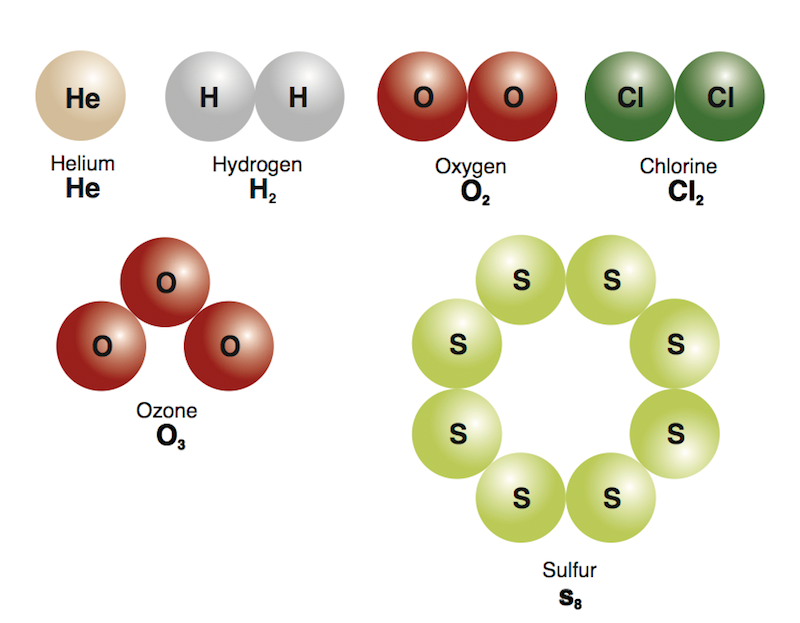
Sedangkan molekul unsur terdiri dari dua atau lebih atom yang sama dalam struktur yang lebih besar. Dengan kata lain, atom-atom penyusunnya memiliki ikatan kimia tetapi memiliki unsur yang sama.
2. Jumlah Unsur Pembentuk
Selain itu, molekul senyawa memiliki lebih dari satu jenis unsur yang berikatan bersama, sehingga membentuk senyawa kimia baru dengan sifat-sifat yang unik. Sedangkan molekul unsur terdiri dari atom-atom tunggal dari jenis yang sama.
3. Sifat Kimia dan Fisik
Terakhir, sifat kimia dan fisik dari senyawa kimia berbeda dari unsur-unsur pembentuknya. Sementara molekul unsur memiliki sifat kimia dan fisik yang mirip dengan unsur-unsur pembentuknya. Molekul unsur masih dapat bereaksi dengan zat lain, tetapi cenderung memiliki sifat yang lebih mirip dengan atom-atom individual.
Ciri-Ciri Molekul Senyawa
Beberapa ciri khas yang dapat mengidentifikasi senyawa kimia dengan senyawa lain antara lain:
- Terdiri dari dua atau lebih jenis atom yang berbeda.
- Atom-atom yang membentuk senyawa memiliki rasio tetap sesuai dengan rumus molekulnya.
- Memiliki sifat fisik dan kimia yang unik, yang membedakannya dari unsur dan senyawa lain.
Sifat dan Karakteristik Molekul Senyawa
Berikut ini adalah penjelasan mendalam mengenai sifat dan karakteristik senyawa kimia:
1. Titik Leleh dan Titik Didih
Senyawa kimia memiliki titik leleh dan titik didih yang spesifik, yang mana berbeda dari unsur-unsur pembentuknya. Penyebabnya adalah senyawa membentuk ikatan kimia yang berbeda, seperti ikatan kovalen dan ionik.
2. Kelarutan
Kemudian, sifat kelarutan molekul senyawa bergantung pada jenis ikatan yang ada di dalamnya. Sebagai contoh, senyawa ionik cenderung larut dalam air karena air dapat membentuk ikatan hidrogen dengan ion-ion yang bermuatan.
Senyawa kovalen polar juga dapat larut dalam air karena gaya antarmolekul yang mirip. Sementara itu, senyawa nonpolar umumnya tidak larut dalam air.
3. Kekerasan dan Sifat Mekanik Lain
Jenis ikatan dan struktur kristal suatu senyawa juga mempengaruhi kekerasannya. Senyawa ionik cenderung keras dan rapuh, sedangkan senyawa kovalen cenderung lembut. Struktur kristal juga dapat mempengaruhi sifat mekanik senyawa.
4. Konduktivitas Listrik
Molekul senyawa dapat bersifat konduktor atau isolator listrik, tergantung pada apakah senyawa tersebut memiliki ion atau elektron bebas yang dapat menghantarkan arus listrik. Senyawa ionik cenderung menjadi konduktor dalam fase cair atau larutan, sedangkan senyawa kovalen nonpolar cenderung menjadi isolator.
5. Reaktivitas Kimia
Selain itu, ikatan kimia suatu senyawa juga menentukan sifat reaktivitasnya. Maksudnya, senyawa dengan ikatan kovalen polar atau ionik cenderung bersifat reaktif dan dapat berpartisipasi dalam berbagai reaksi kimia, termasuk reaksi oksidasi, reduksi, dan asam-basa.
6. Warna dan Bau
Beberapa senyawa memiliki warna dan bau yang khas, terutama senyawa organik. Penyebabnya adalah pada struktur elektroniknya, yang mana dapat menyerap dan memancarkan cahaya pada panjang gelombang tertentu.
Jenis-Jenis Molekul Senyawa
Molekul senyawa dapat dikelompokkan ke dalam beberapa jenis berdasarkan komposisi dan struktur molekulnya. Masing-masing jenis senyawa akan memiliki sifat dan karakteristik unik yang berkaitan dengan jenis ikatan yang terbentuk di dalamnya. Berikut adalah beberapa jenisnya yang umum:
1. Senyawa Organik
Jenis senyawa organik merupakan senyawa yang mengandung karbon (C) dan biasanya memiliki ikatan karbon-karbon (C-C) atau karbon-hidrogen (C-H). Contoh senyawa organik termasuk karbohidrat, protein, lipid, dan asam nukleat.
2. Senyawa Anorganik
Sementara jenis senyawa anorganik umumnya tidak mengandung karbon (C) dan hidrogen (H) yang berikatan dalam ikatan C-C atau C-H. Contoh senyawa anorganik yaitu air (H2O), garam (NaCl), dan asam sulfat (H2SO4).
3. Senyawa Non-organik
Terakhir, kelompok ini mencakup senyawa yang tidak memiliki ikatan C-C atau C-H, dan umumnya berasal dari logam dan nonlogam. Sedangkan contoh senyawa non-organik yaitu natrium oksida (Na2O) dan kalsium klorida (CaCl2).
Contoh Molekul Senyawa, Rumus, dan Unsur Pembentuknya
Pastinya, senyawa-senyawa kimia memiliki rumus kimia yang merepresentasikan unsur-unsur yang membentuknya. Berikut adalah beberapa contoh molekul senyawa beserta rumus kimia dan unsur-unsur pembentuknya:
1. Air (Air Murni)
Senyawa kimia yang paling umum adalah air, juga terkenal sebagai air murni. Selain untuk konsumsi manusia dan hewan, air juga sangat berguna dalam pertanian, industri, dan berbagai proses kimia.
Rumus kimia air adalah H2O, yang mana mengindikasikan bahwa molekulnya terdiri dari dua atom hidrogen (H) yang terikat pada satu atom oksigen (O).
2. Garam Meja (Natrium Klorida)
Sementara garam meja merupakan salah satu contoh senyawa ionik yang umumnya bermanfaat sebagai bumbu makanan dan pengawet dalam industri makanan. Selain itu garam juga penting untuk keseimbangan elektrolit dalam tubuh manusia.
Rumus kimia garam adalah NaCl. Artinya, molekul senyawa ini memiliki satu atom natrium (Na) dan satu atom klorin (Cl).
3. Glukosa
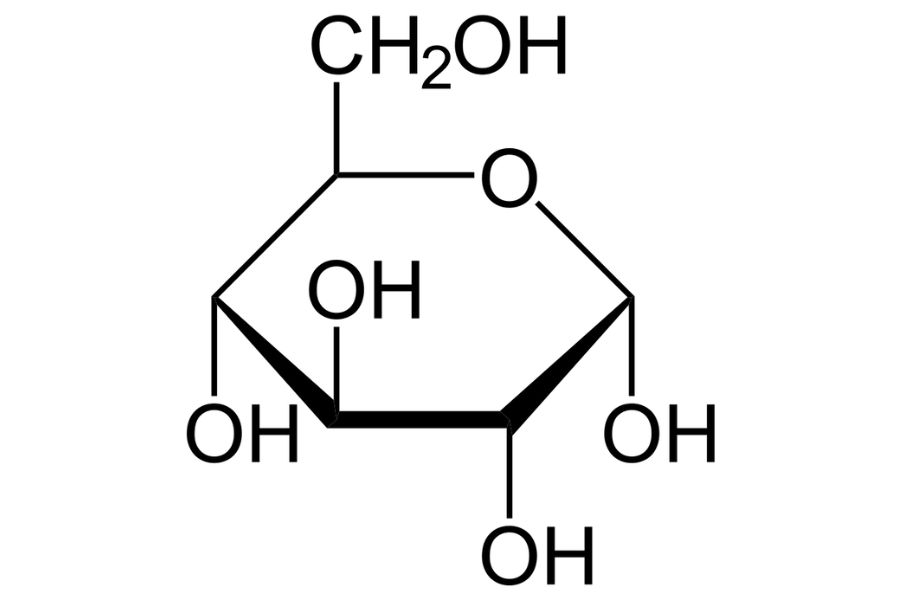
Selain itu, terdapat glukosa yang merupakan bentuk sederhana dari karbohidrat. Glukosa menjadi sumber utama energi bagi makhluk hidup. Namun, glukosa juga sangat berguna dalam industri makanan dan minuman sebagai bahan tambahan.
Rumus kimia glukosa adalah C6H12O6, yang menandakan bahwa glukosa memiliki enam atom karbon (C), dua belas atom hidrogen (H), dan enam atom oksigen (O).
4. Metana
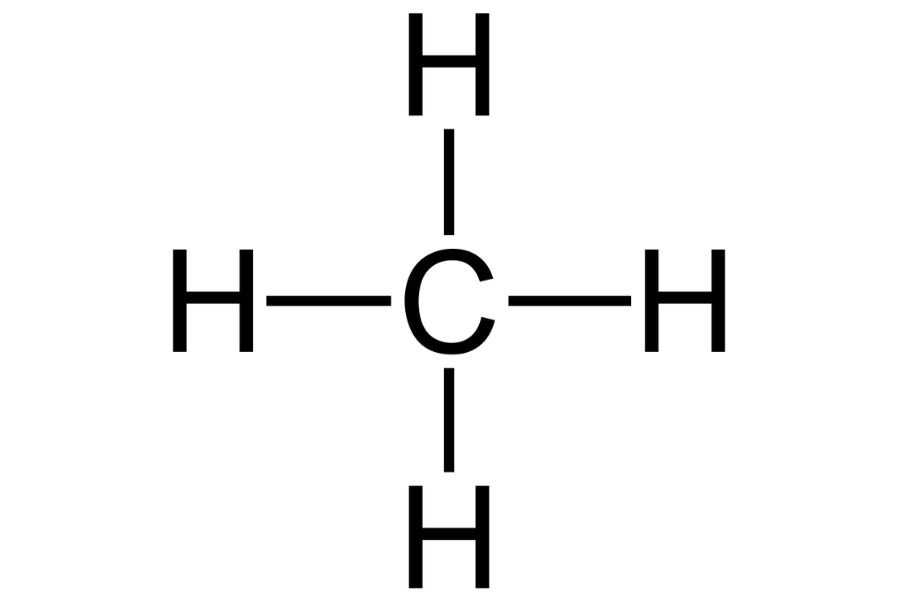
Selanjutnya yaitu metana, yang merupakan senyawa organik paling sederhana. Sebagai gas alam, metana berfungsi sebagai bahan bakar untuk pemanasan dan produksi energi. Selain itu, metana juga sangat penting dalam industri kimia sebagai bahan baku untuk sintesis senyawa organik lainnya.
Rumus kimia metana adalah CH4. Maka artinya, metana terdiri dari satu atom karbon (C) dan empat atom hidrogen (H).
5. Asam Sulfat
Contoh terakhir yaitu asam sulfat, suatu senyawa anorganik yang bersifat sangat kuat. Banyak industri yang menggunakan asam sulfat dalam menjalankan reaksi kimianya. Misalnya untuk produksi pupuk, bahan kimia, dan industri metalurgi.
Rumus kimia asam sulfat yaitu H2SO4, yang menandakan bahwa senyawa ini memiliki dua atom hidrogen (H), satu atom belerang (S), dan empat atom oksigen (O).
Sudah Paham Konsep Molekul Senyawa dan Manfaatnya?
Pada kesimpulannya, pemahaman tentang molekul senyawa memiliki dampak yang luas dan penting. Mulai dari air yang Anda minum hingga senyawa kompleks dalam tubuh manusia, keberadaan dan sifat molekul-molekul ini berperan penting sesuai sifat dan karakteristiknya masing-masing untuk bisa Anda manfaatkan.
Selain contoh-contoh senyawa yang kami sebutkan di atas, masih ada banyak sekali senyawa yang bisa Anda eksplorasi. Dengan mengetahui berbagai senyawa dan manfaatnya, Anda akan bisa mengambil manfaatnya dalam kehidupan. Semoga artikel ini bermanfaat!